Macroglobulinemia de Waldenstrom
Última edición el : 26/09/2024
La enfermedad de Waldenström, o macroglobulinemia de Waldenstrom, es un síndrome linfoproliferativo crónico de células B caracterizado por infiltración linfoplasmocitaria de la médula ósea y la presencia de una inmunoglobulina monoclonal sérica del tipo IgM.
Algunos lo consideran una forma evolutiva de un linfoma no Hodgkin (LNH) de bajo grado. Es el primer diagnóstico a considerar en caso de un pico de IgM en la electroforesis.
Es una enfermedad rara con una incidencia de 0,5 casos por cada 100.000 habitantes por año. Representa alrededor del 2% de las enfermedades hematológicas malignas. La mediana de edad en el momento del diagnóstico es de 63 años, y la relación de sexo es de 2 mujeres por cada hombre.
Existen formas familiares excepcionales, que deben investigarse en pacientes menores de 50 años.
Clínica
En el 40 al 50% de los casos, el diagnóstico se realiza tras el descubrimiento incidental de anomalías biológicas (tasa de sedimentación elevada, hemograma alterado, electroforesis perturbada). En otros casos y durante la evolución, pueden aparecer diversas anomalías clínicas:
- Signos de infiltración tumoral (30-50%)
- Adenopatías (más frecuentemente cervicales-axilares que inguinales), típicamente bilaterales, simétricas, firmes, indoloras
- Hepatoesplenomegalia, generalmente leve (20-30%)
- En el 10%: signos de infiltración orgánica (digestiva, ósea, pulmonar, renal, neurológica, etc.)
- Signos de hiperviscosidad plasmática (~ 15% de los casos, debido a la fijación de moléculas de agua en los residuos de carbohidratos de la IgM y a la alteración de la deformabilidad de los eritrocitos causada por la IgM)
- Síndrome hemorrágico: epistaxis, gingivorragias, hematemesis, etc.
- También por interacción con factores de coagulación, fosfolípidos o plaquetas
- Síndrome de sufrimiento neurológico: cefaleas, alteración del estado de alerta, neuropatías, etc.
- Síndrome hemorrágico: epistaxis, gingivorragias, hematemesis, etc.
- Signos de actividad crioglobulinémica (crioglobulinas de tipo I o II presentes en el 10-15% de los casos, sintomáticas en el 5%)
- Fenómeno de Raynaud, oclusiones vasculares periféricas, púrpura vascular, artralgias, úlceras cutáneas recurrentes, acrosíndrome vascular, neuropatías, nefropatías, etc.
- Signos de insuficiencia medular: palidez, fatiga, disnea
- Signos generales: pérdida de peso, fatiga
- Signos de amiloidosis AL (2% de los casos) con afectaciones cardíacas y pleuropulmonares frecuentes
- Polineuropatías autoinmunes (anti-MA, anti-GM1, actividad antisialosil, actividad antidisacárido de heparina)
Evolución y pronóstico
La evolución habitual es la de una hemopatía linfocítica crónica con recaídas sucesivas: elevación de [IgM], desarrollo progresivo de pancitopenia, complicaciones infecciosas. ~15% de aparición de cánceres asociados. Posible transformación (~5-10%) en linfoma agresivo.
La mediana de supervivencia es de 5 a 10 años con tratamiento. La remisión completa es rara. Los principales factores desfavorables son: edad > 60-70 años, anemia, β2-microglobulina > 3 mg/l, albúmina < 40 g/l, pérdida de peso, bi- o pancitopenia.
Exámenes complementarios
- Biología:
- Velocidad de sedimentación (VS) elevada (una crioglobulinemia puede normalizar la VS), anemia normocrómica normocítica generalmente, rara vez linfocitosis y/o neutropenia, trombocitopenia (40%)
- Proteinemia frecuentemente de 80-120 g/l, actividad crioglobulinémica (15%, mayormente tipo I)
- Β2-microglobulina > 3 mg/l en el 50%, actividad de aglutinina fría en el 10%, LDH aumentada en las formas agresivas, alteraciones en las funciones renales/hepáticas, anomalías frecuentes en la hemostasia
- Electroforesis: pico de IgM
- Inmunoelectroforesis/fijación: pico de IgM (con cadena ligera κ en el 75%)
- Orina: proteinuria de Bence-Jones baja en el 50-60% de los casos
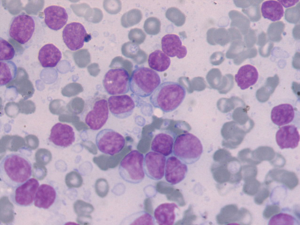
- Mielograma y biopsia osteomedular:
- Médula rica con infiltración (representando del 20 al 100% de las células) linfocítica, linfoplasmocitaria o plasmocitaria polimorfa difusa, y presencia frecuente de mastocitos (26% de los pacientes), discreta mielofibrosis (50%)
- Biopsia ganglionar:
- Invasión difusa de células linfoides y mastocitos, desaparición de la arquitectura normal
- Inmunofenotipado de células linfoides
- Fondo de ojo en caso de (sospecha de) síndrome de hiperviscosidad
Criterios diagnósticos
Todavía en debate. Actualmente se considera la asociación de:
- Pico monoclonal de IgM, independientemente de su magnitud (sin embargo, cuanto mayor sea el nivel, más probable será el diagnóstico)
- Infiltración medular generalmente difusa por pequeños linfocitos con diferenciación plasmocitaria
- Fenotipo tumoral: IgM+, CD5-/+, C10-, CD19+, CD20+, CD22+, CD23-, CD25+, CD27+, FMC7+, CD103-
Diagnóstico diferencial
El diagnóstico diferencial de la enfermedad de Waldenström incluye gammapatía monoclonal de IgM:
- Enfermedad de Waldenström asintomática
- No requiere tratamiento, el tiempo medio de progresión a enfermedad sintomática es de 7 años
- MGUS con IgM
- Linfomas de la zona marginal con componente monoclonal de IgM
- Diagnóstico diferencial difícil (argumentos histológicos, pico de IgM bajo con otros picos, etc.)
- Leucemia linfocítica crónica
- Generalmente caracterizada por hipogammaglobulinemia, pero se observa un pequeño pico de IgM en el 10-15% de los casos
- Crioglobulinemia de tipo IgM
- Enfermedad primaria idiopática de aglutininas frías
- Mieloma múltiple de IgM: raro
- Gammapatías monoclonales secundarias de IgM: infecciones (VEB, CMV, VIH, hepatitis, etc.), enfermedades autoinmunes (LES, AR, Sjögren, tiroiditis, PAN), enfermedades hepáticas cirróticas, glomerulopatías, etc.
- Sindrome de Randall, urticaria crónica con IgM (Schnitzler), enfermedad de cadenas pesadas, etc.
Manejo terapéutico - Tratamientos
Criterios para iniciar tratamiento (enfermedad sintomática):
- Síntomas generales (sudores, fiebre, deterioro general) o síntomas relacionados con la actividad perjudicial de la IgM (ver supra)
- Hb < 10 g/l o Plaquetas < 100.10^9/l o masa tumoral importante (reflejada por los niveles de β2-microglobulina)
Un nivel elevado de IgM no es un criterio terapéutico pero requiere una búsqueda exhaustiva de manifestaciones clínicas (¿síndrome de hiperviscosidad?, ¿hemorragias retinianas o exudados en el fondo de ojo?).
El manejo se basa en el tratamiento sintomático de las complicaciones, la plasmaféresis (++ como tratamiento adyuvante en casos de afectación orgánica progresiva), la quimioterapia (clorambucilo, fludarabina, 2CDA con o sin anticuerpos monoclonales), y los trasplantes de médula ósea autólogos o alogénicos. Aunque no se ha demostrado superioridad, estas moléculas también pueden combinarse o combinarse con un inmunosupresor (ciclofosfamida) o corticoides.
Bibliografía
EMC, traité d'hématologie, Elsevier, 2018
Jameson JL et al., Harrison's Principles of Internal Medicine, 20th edition, McGraw Hill Higher Education, 2018